Bio-Share | 无菌灌装的污染控制策略---欧盟无菌附录新版解析
发布时间: Oct 14 , 2022

无菌生产企业,无论是致力于出海的企业,还是服务于国内生产的企业,都高度关注无菌法规的变化。
2022年8月欧盟正式发布了姗姗来迟的无菌附录一。一经发布,引起了行业内的高度关注,因为该法规代表了未来国内外药政当局对于无菌产品的监管要求。国内GMP和欧盟GMP高度同源,按照此规律,在该欧盟GMP法规执行之后,国内GMP法规很有可能会随之改变,旨在提高行业的无菌认知和无菌保证水平。
在该草案中,最引起大家注意的是,提出了污染控制策略(Contamination Control Strategy,CCS)的概念。污染控制策略(CCS)的定义是:为确保工艺性能和产品质量,从对现行产品和工艺的理解上所设计的一套对微生物、热原和微粒的控制系统。
包括原液/原料药、辅料、药品和组分、设施和设备操作条件、环境控制、过程控制、成品质量标准相关的参数和属性,及相关的监控的方法及频次。
在草案中,共有多达51处提到了CCS控制策略,是出现频次最高的词汇之一,出现的章节分别如图所示。
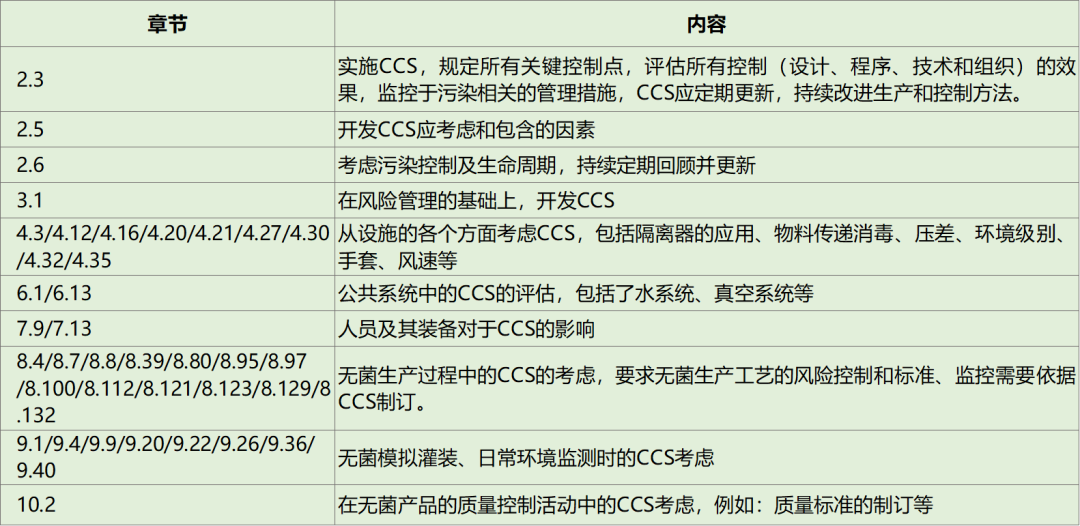
表1.CCS控制策略章节展示(点击图片可放大浏览)
CCS控制的对象是微生物、微粒和热原,这三个对象也是无菌产品控制的主要挑战。
产品污染、未能建立和维持微生物和微粒污染的有效控制措施,一直是美国市场药品召回和实施法规监管行动的主要原因,也是产品召回、市场抽检不合格和法规监管缺陷的主要来源。
那么如何去实现CCS控制策略呢?PDA在2021年11月17日发布了关于CCS污染控制策略的Q&A,从“预防、补救、监督和持续改善”给出了以下建议:

图1.CCS污染控制策略建议
01 预防
预防是污染控制的最有效手段。防止污染物到达关键工艺区域应当是污染控制策略的目标。完全预防并不总是可行,但是,它应该成为每个工厂持续改进的目标。
预防策略应包括建立一个明确的、有组织的程序,从对无菌产品生产工艺的良好理解开始,针对工艺变更和污染源进行客观的风险评估,制定可实现的验收标准和指标,也就是监控的性能及根据需要调整策略的方案。
02 补救
成功的CCS的第二个重要支柱是补救。补救是由于预防措施不足或限制,而对污染事件做出的反应。补救包括评估或调查污染源,并采取维持或使工艺恢复受控状态所需的具体措施即CAPA(Corrective Actionsand Preventive Actions,纠正预防措施)。
03 监测和持续改进
了解预防和补救策略的有效性,对于污染控制和过程改进同样重要。应对关键污染控制参数进行监测评估,使它能够评估控制的有效性。对于更关键的参数,如洁净室压差和总微粒数,可能需要连续监测。
持续改进措施遵循科学的生命周期规则,并与公司的制药质量体系(Pharmaceutical Quality System,简称:PQS)结合。CCS一旦实施,就需要定期维护,并将其作为定期产品质量审核的一部分,以确保投入的物品、设施的设计或生产过程中的任何变化,都已按照CCS和PQS实施。
所以,CCS的实施,不是一次性达到目的。它是实现控制状态的手段。它不仅反映了当前的控制状态,而且还带来了对新技术、新方法的需求的认知。这些新技术或方法可以弥补差距。
在制药行业的法规标准要求越来越严格的情况下,“人”作为无菌污染的最大来源,对人员风险控制除了建立并保持良好的质量保证系统、配备足够数量并具有适当资质的人员完成各项操作,生产操作人员应掌握微生物的基本知识,养成良好的卫生习惯等基本的方法外,生产的连续性和阶段式生产能有效地降低人员和生产操作导致污染的风险。
图2.康日百奥Bioworkshops冻干产线实拍图
在药品灌装生产中,无菌是非常重要的控制因素也是最重要的一个环节。作为一家大分子CDMO,康日百奥的质量体系按照FDA,EMA,NMPA法规要求,参考PIC/S,ICH等指导原则,建立完善的且符合国际化要求的质量管理体系。
康日百奥可实现0.2mL-5.0mL不同制剂规格的卡式瓶、预充针的高效切换及连续生产;康日百奥引入了智能化的无菌预灌封系统,借助2个超洁净无菌机器人手臂,减少污染风险和人为变量,完全实现了灌装的高精度,提供了稳定的无菌保障,年产能为1000万瓶。

图3.康日百奥超洁净无菌机器人手臂实拍图
除了无菌预充针、卡式瓶灌装线外,康日百奥同时可提供无菌水针西林瓶,冻干西林瓶(2,6,8,10,15,20,50R)临床前及商业化成品的灌装服务,产能达到1500万支/年,可完全灵活满足合作伙伴对于不同工艺,不同类型制剂产线的灌装量日益增长的需求。
为了增加安全性,灌装产品会进行严格的分析筛选和质量控制。康日百奥拥有完善的无菌保障体系,更衣确认、人员资质、烟雾流型测试、灭菌工艺确认、培养基模拟灌装等均严格按照法规要求,同时完整的QC检测放行体系,稳健的分析能力,可以确保交付产品的及时检测/放行。

康日百奥质量管理体系框架基于生物制药全生命周期质量管理的要求,并结合风险管理、质量源于设计等理念。
体系涵盖了厂房设施设备管理,人员资质管理,原辅料的管理、药品生产、检验、放行、运输和发运的全过程,验证管理等。全面帮助客户确保药品生产过程中的安全性和合规性,严格把控过程中的每一道关。
【西林瓶(水针+冻干)、预充针、卡式瓶无菌灌装服务】
康日百奥无菌制剂灌装生产车间,拥有包括D级区、C级区和B级区以及B+A环境下的无菌灌装区域,所有质量体系已通过:欧盟质量受权人审计、FDA第三方审计,并取得药品生产许可证。
康日百奥拥有西林瓶(水针+冻干)、预充针、卡式瓶等市场上主要药物剂型的无菌灌装生产线,灌装产量达1500万支/年。
目前可灌装品种包括抗体、融合蛋白、疫苗等多种生物制剂,所有会影响产品生产的过程、文件、人员、环境、物料都会进行严格监控。
基于强有力的法规支持,针对无菌灌装完备的QC检测放行体系,可为合作伙伴高效高质灵活的提供无菌制剂灌装服务。
商业化西林瓶(水针+冻干)线
√可以为(2,6,8,10,15,20,50R)规格的水针、冻干制剂提供高效的灌装服务;
√8针头灌装,灌装精度可以稳定控制在±1%;
√单次批量最大:100,000瓶,年水针产量可达400万瓶;配置有全自动进出料系统冻干产能可达100万瓶/年。
无菌预充针、卡式瓶灌装线
√可实现0.2mL-5.0mL不同制剂规格高效切换及连续生产;
√康日百奥引入了智能化的无菌预灌封系统,借助2个超洁净无菌机器人手臂,完全实现了灌装的高精度,提供了稳定的无菌保障,年产能为1000万支。
















