Bio-Share | 双特异性抗体生物测定开发考量
发布时间: Jul 04 , 2022
双特异性抗体通过结合两个抗原靶点,实现一加一大于二的疗效。但由于其复杂的作用机制、不同的结构变化和双靶点结合,开发生物测定方法和其他类型的分析方法来表征双特异性抗体是具有挑战性的。本文梳理开发生物学测定方法,需要重点考量的三个因素。
生物测定方法开发与药物开发阶段相适应
分阶段开发和实施生物测定的方法是行业和监管机构广泛接受的策略,类似的原则也适用于双特异性抗体药物开发。
产品开发的早期阶段,通常使用的方法是结合实验(Binding Assay),其中最常用的包括酶联免疫吸附实验(ELISAs)或表面等离子体共振(SPR)技术。
产品开发的后期阶段,通常使用可以反映双特异性抗体作用机制(Mechanisms of Action, MoA),更为复杂的方法,上市申请递交之前进行验证。但是一般建议更早开发基于MoA的相关生物测定方法,这样可更大程度了解工艺和产品,而且可在关键临床试验之前更好地了解该方法的性能。
临床阶段,需要使用基于细胞的生物测定方法,监测关键步骤和成分的生物学效应。
生物测定方法的开发是基于表征MoA的需要。如果MoA只需要与靶点结合,一种替代方法,如蛋白质结合或竞争性结合试验,可能足以确定效力。而开发可靠的和QC适用的,开发基于细胞的生物测定方法比基于非细胞的结合分析方法更具挑战性。
生物测定方法开发与药物作用机制相符合
生物测定的设计策略是由药物预期的MoA决定的,一种设计良好的生物测定方法不仅准确可重现,而且能够充分反映药物的作用机制。
在双特异性抗体开发过程,可能涉及开发双重、三重协同MoAs的生物测定方法。在某些情况下,一个分子中存在多种作用机制,优先使用单一分析模型来测量所有MoAs的方法用于产品放行和稳定性测试。如果需要,可以开发多种活性表征分析方法,例如:细胞杀伤,细胞因子分泌,ADCC,ADCP等来充分的评估分子的生物活性。
四种常见的MOA及生物测定方法
1.细胞桥接(Cell-bridging BsAbs)
最常见的是T细胞双抗,包括一个anti-CD3抗体臂和一个anti-TAA抗体臂。T细胞双抗桥接靶细胞和T细胞,形成免疫突触,诱导T细胞激活,释放穿孔素,颗粒酶B等裂解靶细胞。
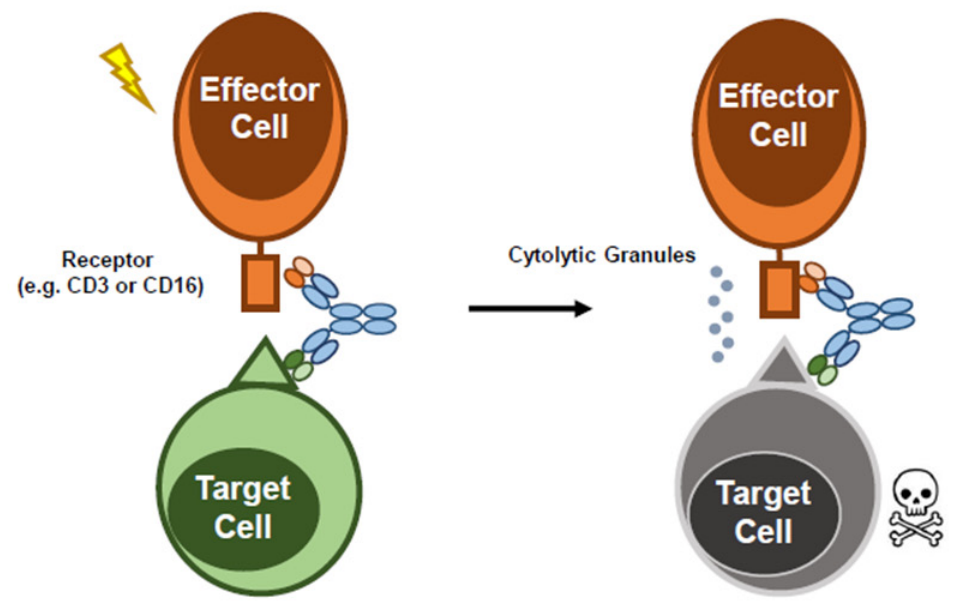
相关生物测定方法
1.结合实验:任何基于抗体技术的药物,结合实验都是基础。通常使用ELISA法和SPR法。
2.生物活性测定:T细胞双抗是效应细胞和靶细胞形成免疫突触,进而活化,杀伤靶细胞。优化的报告基因法检测效应细胞激活,以及细胞杀伤实验检测靶细胞的杀伤效果,是常用的生物活性测定实验。
3.其他功能测定:通过流式细胞术检测细胞因子、颗粒酶、穿孔素等。
2.配体-受体结合(Receptor/Ligand BsAbs)
这类双抗靶向多个受体,激活受体(如现在流行的双激动抗体)或者阻断受体功能(如双免疫检查点抗体)。
PD-1XCTLA4双抗是目前国内最拥挤的双抗管线(如康方生物AK104),通过阻断PD-1/PD-L1,CTLA-4/CD80的结合,从而恢复T细胞功能。
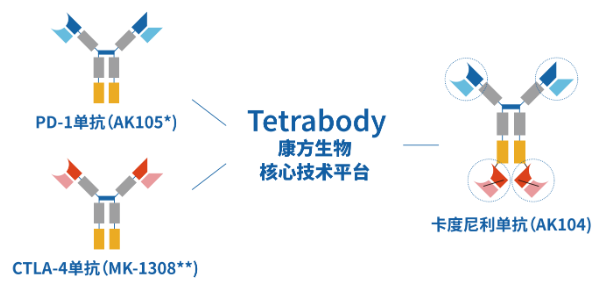
康方生物官网
生物测定方法
1.结合实验:使用ELISA和SPR法进行单靶点和双靶点的结合实验。
2.生物活性:受体激活或阻断后的细胞活性变化,如增殖,凋亡,细胞因子释放等。
3.其他功能研究:如激活或阻断受体后,下游激酶活性改变,钙流变化等
4.效应功能:CDC、ADCC、ADCP、FcγR结合等
3.辅助因子模拟(Cofactor Mimicking BsAbs)
罗氏的Emicizumab (Hemlibra®),是一种用于治疗A型血友病的双特异性抗体,与凝血因子X和IX结合,因此能够发挥凝血因子XIII的作用。

生物测定方法
1.结合实验:使用ELISA和SPR法进行单靶点和双靶点的结合实验
2.生物活性:FXa活性
3.其他功能研究:凝血酶生成分析
4.归巢双抗
归巢双抗的一个抗体臂负责将分子带到特定的、通常难以到达位置(如跨越血脑屏障),另外一个抗体臂作用于治疗靶点。
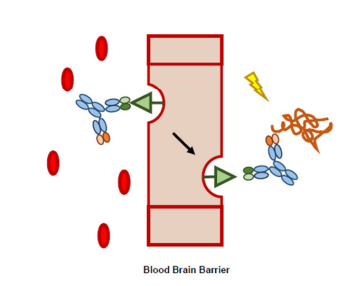
生物测定方法
1.结合实验:BLI及竞争法ELISA。
2生物活性:归巢抗体之外分子的生物活性。
3.其他功能研究:荧光示踪检测双特异性抗体在体内和细胞内分布等 。
整体双特异性抗体表征策略
BsAbs的有效性和安全性评估依赖于系统的表征和生物测定方法开发,可反映这些双靶向抗体的生物活性,并区分更高阶的结构、效价和疗效,包括整体稳定性、片段/聚集、免疫原性、抗原特异性、亲和力、生物活性等。
生物分析方法还可以进行免疫原性和PK/PD评估,以确定双特异性抗体的的安全性和有效性。免疫原性是宿主对治疗性双特异性抗体不必要的免疫反应,会清除抗体,改变PK,降低治疗效果等。免疫原性通过检测抗药物抗体进行临床评估,包括IgM、IgG、IgE和/或IgA等。
用于评估免疫原性的生物测定包括结合免疫测定,如ELISA检测所有能够结合治疗性双特异性抗体的ADA,以及针对生物活性位点的中和分析(体外细胞分析或竞争性配体结合分析),MHC-II相关肽蛋白质组学(MAPPs)检测可以表征抗体免疫原性片段。生物制剂的PK至少部分地由FcRn介导的再循环决定。体外通过SPR等监测双特异性抗体Fc与FcRn的结合能力,评估对PK的潜在影响。
小结
双特异性抗体作用机制复杂,通过系列完整的生物测定方法,表征双特异性抗体药物关键质量属性,生物学活性等,以确保在临床阶段,双特异性抗体能够充分发挥其MoA的活性,起到治疗效果。生物测定采用的方法与药物开发阶段相关,其中MoA相关生物活性测定是重中之重,也是开发难点,因而应该从双抗项目开发最初阶段,同步建立对应的生物测定方法,才能保证双抗项目的稳步推进。选择有相关项目经验的CDMO企业,可以保证双抗工艺开发和生物测定方法开发的同步性和一致性,加速项目进展。

康日百奥分析实验室拥有Thermo Orbitrap Exactive HF-X液质联用仪,Thermo Vanquish UHPLC, Protein Simple Maurice, SCIEX PA800 plus, Waters ACQUITY H Class UPLC, Thermo CAD检测器, Malvern全自动毛细管差示扫描量热仪,Octet分子间相互作用仪,MD M5酶标仪,Roche480 qPCR仪等先进研究和检测设备,可对单克隆抗体,双抗,融合蛋白,ADC等生物药进行分析方法开发、确认和验证,并提供全面的蛋白表征研究(包含工艺可比性研究,生物类似药的相似性评价等)。
康日百奥提供完善的细胞株开发,工艺开发,工艺表征、验证,原液生产,无菌灌装等服务,在客户双抗项目开发最初阶段,康日百奥同步建立生物活性测定方法,科学有效的推动客户双抗项目的稳步进行。康日百奥目前已经交付了多个双特异性抗体的细胞株构建以及临床前药学研究的项目,对于双抗(对称+非对称)的工艺开发和生产具有丰富的经验,在合作伙伴Discovery阶段更早的对接药学开发平台,可帮助合作伙伴缩短开发周期,减少项目CMC阶段开发的风险,以稳健的工艺,高效的生产将分子快速的推进临床。
参考文献
1. Register, A.C.; Tarighat, S.S.; Lee, H.Y. Bioassay Development for Bispecific Antibodies—Challenges and Opportunities. Int. J. Mol. Sci. 2021, 22, 5350
2. Dickopf, S.; Georges, G.J.; Brinkmann, U. Format and geometries matter: Structure-based design defines the functionality of bispecific antibodies. Comput. Struct. Biotechnol. J. 2020, 18, 1221–1227
3. Steiner, G.; Marban-Doran, C.; Langer, J.; Pimenova, T.; Duran-Pacheco, G.; Sauter, D.; Langenkamp, A.; Solier, C.; Singer, T.; Bray-French, K.; et al. Enabling Routine MHC-II-Associated Peptide Proteomics for Risk Assessment of Drug-Induced Immunogenicity. J. Proteome Res. 2020, 19, 3792–3806
















