Bio-Share | 双特异性抗体开发关键技术考量
发布时间: Jun 23 , 2022

1983年MRC的科学家Milstein,C.和牛津大学的Cuello, A. C开创双特异性抗体技术Quadroma,至今已有40年。在科学家不断的努力之下,双特异性抗体终于获得突破,过去1年有3款产品上市,分别是杨森的amivantamab-vmjw/Rybrevant™(EGFR/c-Met),罗氏的faricimab-svoa/VABYSMO™(Ang-2/VEGF-A)和mosunetuzumab(CD3/CD20)。
双特异性抗体,根据不同生物学活性需求,不断衍生出新的format,至今已有超200种,如何选择是关键技术考量之一。双特异性抗体由两个不同的抗体合二为一,但是每一种抗体亲和力要求不同,优化亲和力,实现平衡是关键技术考量之二。
从上市产品看Format选择
经过四十年的开发,逐渐积累超过200种不同的Format,总体上可以分为IgG样format, 和片段化抗体Format(非IgG样format)。如何选择,或者如何在此基础上衍生出新型format是双特异性抗体开发技术考量之一。
IgG样双抗
最近上市的三款产品采用了IgG样的Format。
杨森的amivantamab(EGFR/c-Met)采用了Genmab的 DuoBody技术平台,该技术分三步:第一步,使用重组哺乳动物表达系统分别产生两个IgG1, 其CH3结构域分别包含1个突变(409位赖氨酸到精氨酸,K409R;405位苯丙氨酸到亮氨酸F405L)。第二步:纯化2种IgG1。第三步:两个半IgG1,受控的Fab臂交换(Controlled Fab-arm exchange),组装成双特异性抗体。
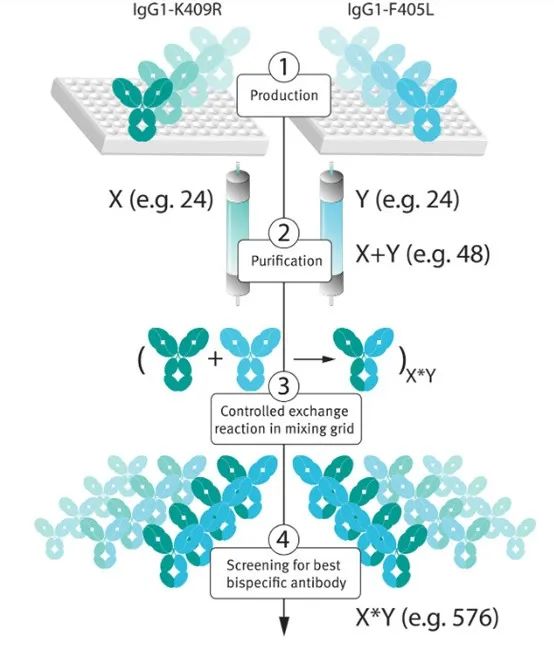
罗氏的Faricimab(Ang-2/VEGF-A)采用了自己的CrossMab技术平台,是其knobs-into-holes技术的升级版。
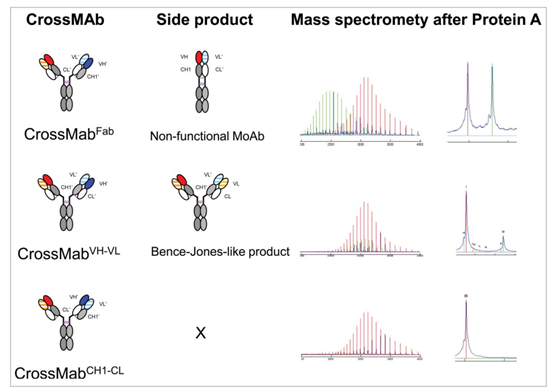
mAbs 2021
CrossMab从2011年开发,经历了多次演化。CrossMabFab技术,将原重链VH-CH1结构域与轻链VL-CL与进行互换,这个工艺会产生MoAb和Fab副产物;CrossMabVH-VL是将抗体的VL和VH进行互换,会产生Bence-Jones样 Mab副产物;为了避免该副产物的形成,罗氏鉴定了Fab中的自然电荷对,并将各自的正交电荷相互作用引入非交换抗体CH1-CL结构域,由于排斥电荷相互作用,Bence-Jones Mab副产物不会产生,则称为 CrossMabCH1-CL。
最近上市的mosunetuzumab(CD3/CD20)则采用了其经典knobs-into-holes技术,1996年Genentech的Carter和他的同事基于此开发了双抗重链组装的KIH技术,Knob是小氨基酸被大氨基酸替换(如T366W),将其插入到Hole(大氨基酸被小氨基酸替换)中,这是第一个进行双抗重链组装的技术平台。
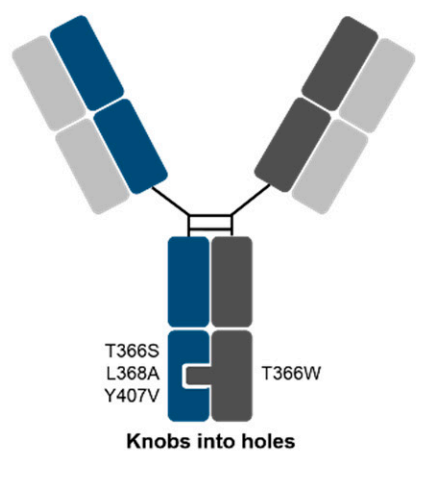
Antibodies 2018
除了上述已经上市产品使用的技术平台之外,还有Zymeworks 公司的Azymetric™技术,Merck的SEED技术,康方生物的Tetrabody技术等,都是非常有特点的IgG样双抗技术平台。
IgG样双抗,因为结构上和IgG单抗类似,工艺及半衰期等与经典的单抗药物类似。但是IgG样分子比较大,组织穿透能力弱,对于实体瘤等,可能会存在穿透力弱引起的效力低等问题,因而片段化抗体,甚至是单域抗体串联组成的小分子双特异性抗体format也被开发出来。
非IgG样双抗
BiTE(bispecific T-cell engager)
非IgG样双抗,比较经典的是BiTE,基于此技术的开发的Blincyto®(blinatumomab,Amgen)2014年获得FDA批准,2015年获得欧盟批准,2020年12月8日中国批准上市,商品名:倍利妥(贝林妥欧单抗),用于治疗成人复发或难治性前体 B 细胞急性淋巴细胞白血病。
BiTE最早由Micromet公司(.2012年被Amgen以11.2亿美金收购)开发,通过多肽连接子(GGGGS)将CD3抗体scFv与TAA抗体的scFv串联而成。BiTE的分子量约55KD,组织穿透力强,但是半衰期小于2小时。现在新一代的half-life extended (HLE) BiTE®,多串联了一个Fc结构域,用于延长半衰期。
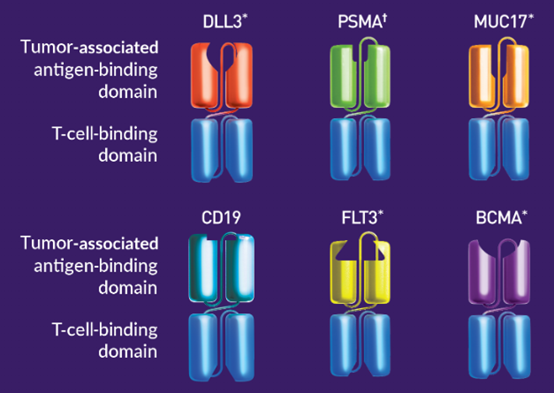
Amgen官网
DART(dual-affinity retargeting)
DART是由MacroGenics开发技术平台2个VL结构域和2个VH结构域通过二硫键连接,尾部带正负电荷,有助于异二聚体形成。分子量56KD,半衰期数小时。MacroGenics也在基础DART分子是加Fc,延长半衰期至数天数周,呈IgG样结构。
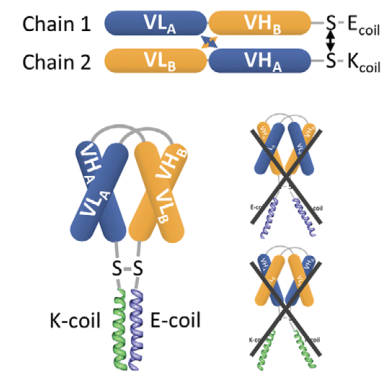
Curr Protoc Immunol . 2020
除上述两种片段化抗体串联双抗平台之外,由Affimed 公司开发ROCK® (Redirected Optimized Cell Killing,重定向优化细胞杀伤)平台,产生四价多特异性抗体也很有特色,分子量大约110KD介于IgG样双抗和BiTE之间。
片段化抗体,具有分子量小,穿透性强的优点,同时也有半衰期短的缺点,通常都会增加一个Fc结构域延长半衰期。
抗体亲和力
与传统的抗体治疗一样,双特异性抗体亲和力是其药理特性的关键决定因素之一。抗体亲和力依据不同的生物学活性而不同,比如通常CD3双抗,CD3抗体臂需要低亲和力,避免过度激活T细胞,一般而言,TAA臂需要高亲和力,以便识别相应的恶变细胞。亲和力由Format,连接子,母本抗体Fv/scFv本身的亲和力,Fv/scFv的数量,format形成的空间位阻等众多因素决定,因而优化亲和力是一个系统工程设计。
例如,不同双抗结构和Format会影响亲和力,因而亲和力的生物学需求,也会决定抗体结构设计。比如scFv和Fv具有不同的亲和力,连接scFv的多肽连接子(peptide linker)会影响亲和力。
基于DART技术(两个Fv)的CD19XCD3双抗介导的最大细胞毒性水平显著高于BiTE技术(两个scFv)CD19XCD3双抗(约2倍)。而获得50%最大效应 (EC50)所需的浓度低达60倍。
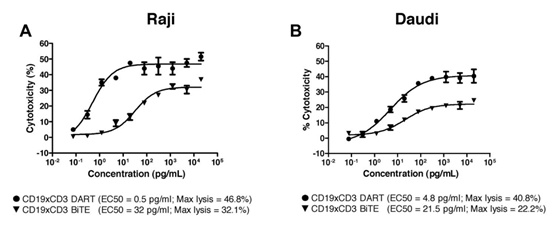
Blood 2011
而AFM11( CD19×CD3 TandAb)是四价抗体,其半衰期长,亲和力较优。
同样是BiTE技术构建CD19XCD3双抗,如果anti-CD3 scFv位于分子的C端(如VLCD19-VHCD19-VLCD3-VHCD3)则亲和力弱,而anti-CD19亲和力不受连接顺序影响。
linker对于亲和力的影响是多方面的,比如对于DVD-Ig的系统研究显示,连接子越长,近端Fv的亲和力越强,使用基于CH1-CH2铰链序列的连接子优于V-C连接序列或聚甘氨酸。
除此之外,连接子的灵活性、靶抗原的大小和结构、表位的位置以及结合相互作用的方向等,都会影响双抗亲和力。
总结
双特异性抗体通过将两个抗体合二为一,产生一加一大于二的疗效,或者显著降低两个单抗联合使用的毒性(如PD-1/CTLA-4双抗)。但是,双特异性抗体构建的复杂程度也远远高于单克隆抗体,如上述,不同的双抗结构format,会影响抗体的亲和力,会产生不同副产物,需要不同的生产工艺和纯化工艺,其细胞株构建的难度以及工艺开发的难度,也远远高于单克隆抗体。
目前,各大生物技术公司研发管线上均可看到双特异性抗体以及多特异性抗体的布局,但从分子构型到最终成药生产,在生产工艺与质控方面均会面临很多挑战。在工程抗体设计日新月异的情况下,如何对抗体的生产工艺进行合理开发,对于质量进行有效控制,成为了多特异性抗体药物临床前开发的重点。市场上涌现出包括康日百奥在内的CDMO企业,提供完善的细胞株开发,工艺开发,产品表征,生产服务整体服务,解决了蛋白表达和质量的优化,产品相关杂质的优化空间和去除能力,鉴定分析副产物,科学有效的指导双特异性抗体的开发。
康日百奥拥有经验丰富的工艺开发团队,在细胞株构建及细胞培养、工艺开发、工艺表征验证等各个环节,团队将参与关键指标的评估。这对于生物药的开发、生产和商业化都至关重要,细胞株构建方面,康日百奥可以提供ATCC CHO-K1,Merck CHOZN-K1等具有清晰溯源的多平台宿主细胞,通过对关键质量属性的关注,构建稳健的细胞株构建平台,致力于为客户的生物药开发提供高质量的符合cGMP要求的细胞株建库服务。
康日百奥已经交付了多个双特异性抗体的细胞株构建以及临床前药学研究的项目,对于双抗(对称+非对称)的工艺开发和生产具有丰富的经验,在合作伙伴Discovery阶段更早的对接药学开发平台,可帮助合作伙伴缩短开发周期,减少项目CMC阶段开发的风险,以稳健的工艺,高效的生产将分子快速的推进临床。
参考文献
1. Milstein C, Cuello AC. Hybrid hybridomas and their use in immunohistochemistry. Nature 1983;305:537-540.
2. Duobody技术平台:https://www.genmab.com/research-innovation/antibody-technology-platforms/
3. Marlena Surowka, Wolfgang Schaefer & Christian Klein (2021) Ten years in the making: application of CrossMab technology for the development of therapeutic bispecific antibodies and antibody fusion proteins, mAbs, 13:1, 1967714, DOI: 10.1080/19420862.2021.1967714
4. Ridgway, J.B.; Presta, L.G.; Carter, P.‘Knobs-into-holes’ engineering of antibody CH3 domains for heavy chain heterodimerization. Protein Eng. Des. Sel. 1996, 9, 617–621
5. Simon Krah et al, Engineering IgG-Like Bispecific Antibodies—An Overview, Antibodies 2018, 7, 28; doi:10.3390/antib7030028 .
6. Ling Huang et al, Multispecific, Multivalent Antibody-Based Molecules Engineered on the DART® and TRIDENT TM Platforms, Curr Protoc Immunol . 2020 Jun;129(1):e95.
7. Moore, P.A.; Zhang, W.; Rainey, G.J.; Burke, S.; Li, H.; Huang, L.; Gorlatov, S.; Veri, M.C.; Aggarwal, S.; Yang, Y.; et al. Application of dual affinity retargeting molecules to achieve optimal redirected T-cell killing of B-cell lymphoma. Blood 2011, 117, 4542–4551.
















